| Qué poca afinidad tienen algunos! |
|
El otro día charlando con uno de vuestros compañeros surgió una cuestión. ¿Por qué el Nitrógeno atómico tiene una afinidad positiva y tan distinta a la de sus vecinos de la tabla periódica? (mira que hay temas interesantes para hablar, pero bueno...). Lo podeis ver en la siguiente imagen.  ¿Quereis saber por qué ocurre? pues hay que seguir leyendo. La respuesta está en la configuración electrónica del Nitrógeno que es [He] 2s2 2p3. Es decir, que en la última capa, de los 6 electrones que caben en el orbital 2p, tenemos la mitad. Esta configuración es muy estable debido a la regla de Hund, que dice que la configuración electrónica de un átomo es más estable cuando tiene electrones desapareados (espines paralelos) que cuando los tiene apareados (espines opuestos o antiparalelos). La razón está en el principio de exclusión de Pauli y en el hecho de que los estados para fermiones idénticos tienen que ser antisimétricos ante el intercambio de dos fermiones idénticos. Cuando los espines están desapareados (paralelos) como la parte de espín es simétrica la parte espacial de la función de onda será antisimétrica, de modo que los dos electrones estarán más alejados y sufren menor repulsión electrostática (para una función de onda simétrica los electrones tienen mayor probabilidad de estar en el mismo punto, por lo que la repulsión electrostática es mayor). Como en el orbital 2p del nitrógeno caben 6 electrones y sólo tenemos 3, la parte de espín de estos electrones puede ser |+++> o |--->, dando lugar a un estado muy estable. En cuanto metamos otro electrón se fastidia esta configuración tan simétrica de la parte de espín, dando lugar a un estado menos estable. Por eso el Nitrógeno no quiere un electrón ni loco. Si os fijais en la tabla anterior, a casi todos los elementos de la columna del Nitrógeno les ocurre lo mismo (aunque en menor grado) y es que tienen una afinidad electrónica menos negativa que sus vecinos de fila y es que todos esos elementos tienen, como el nitrógeno, el último orbital p medio lleno (o medio vacío). |
| Actualizado ( Jueves, 05 de Marzo de 2009 11:44 ) |


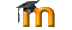





PD: ESCRIBO ESTO CON LA DERECHA MIENTRAS SOTENGO MI PENE SEMI ERECTO CON LA IZQUIERDA.
anonimo
Nada mas solo eso
más que en la existencia de tener una capa completa más y el doble de átomos y por tanto de electrones. Asique, ¿por qué es tan especial el nitrógeno dentro de esta rara familia?, ¿Que le hace más especial que el resto?
Un saludo haters ! Viva diego sorando, es el puto jefe señores. CONCUD MANDA !